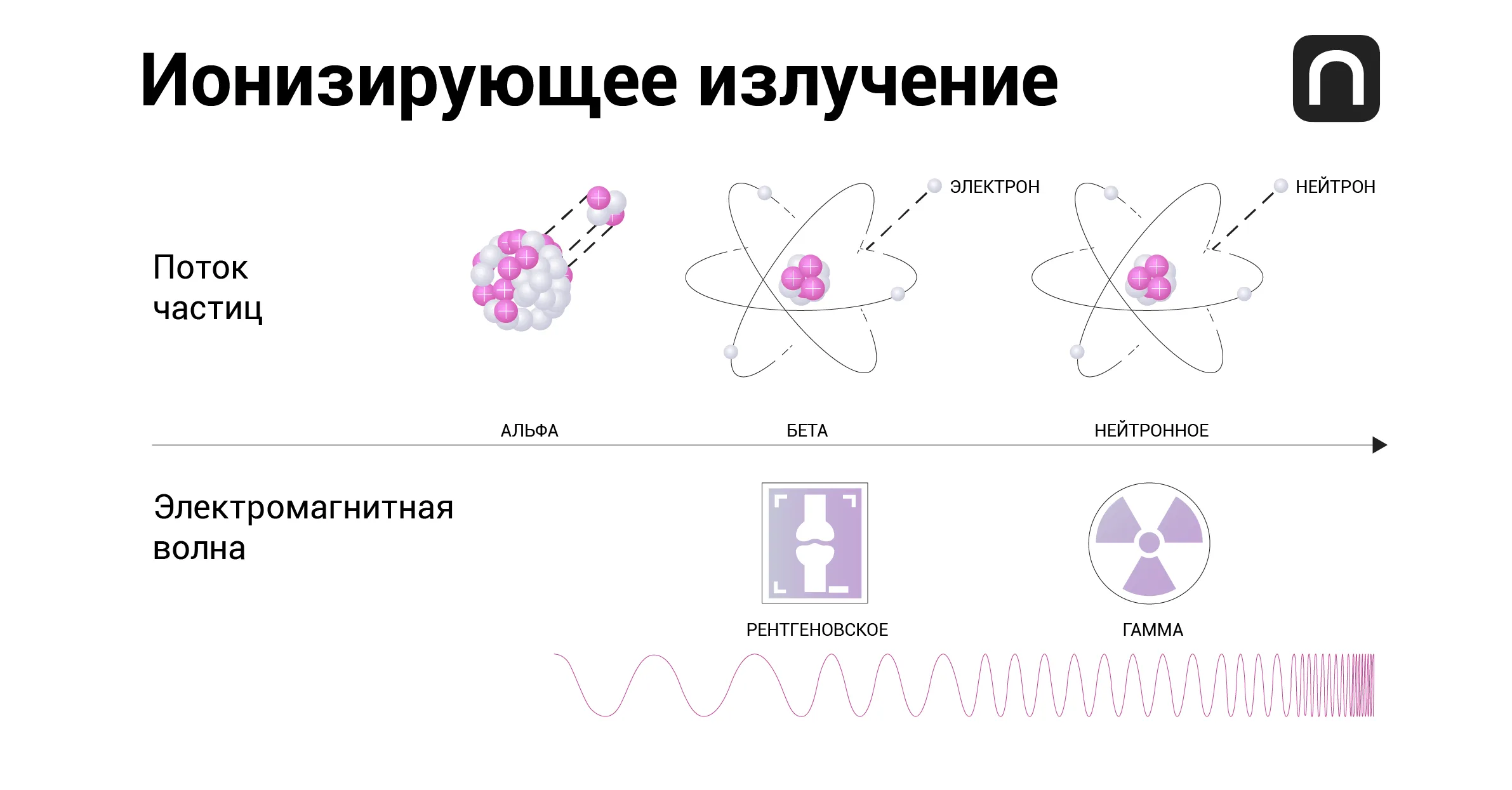
Изотопы — химически почти неразличимые вещества, ядра которых имеют одинаковое число протонов, но разное число нейтронов. Все элементы в таблице Менделеева до 82-го (свинца) имеют как стабильные, так и радиоактивные изотопы. Например, в природе есть два стабильных изотопа водорода — обычный и тяжелый (дейтерий), а также один радиоактивный — тритий.
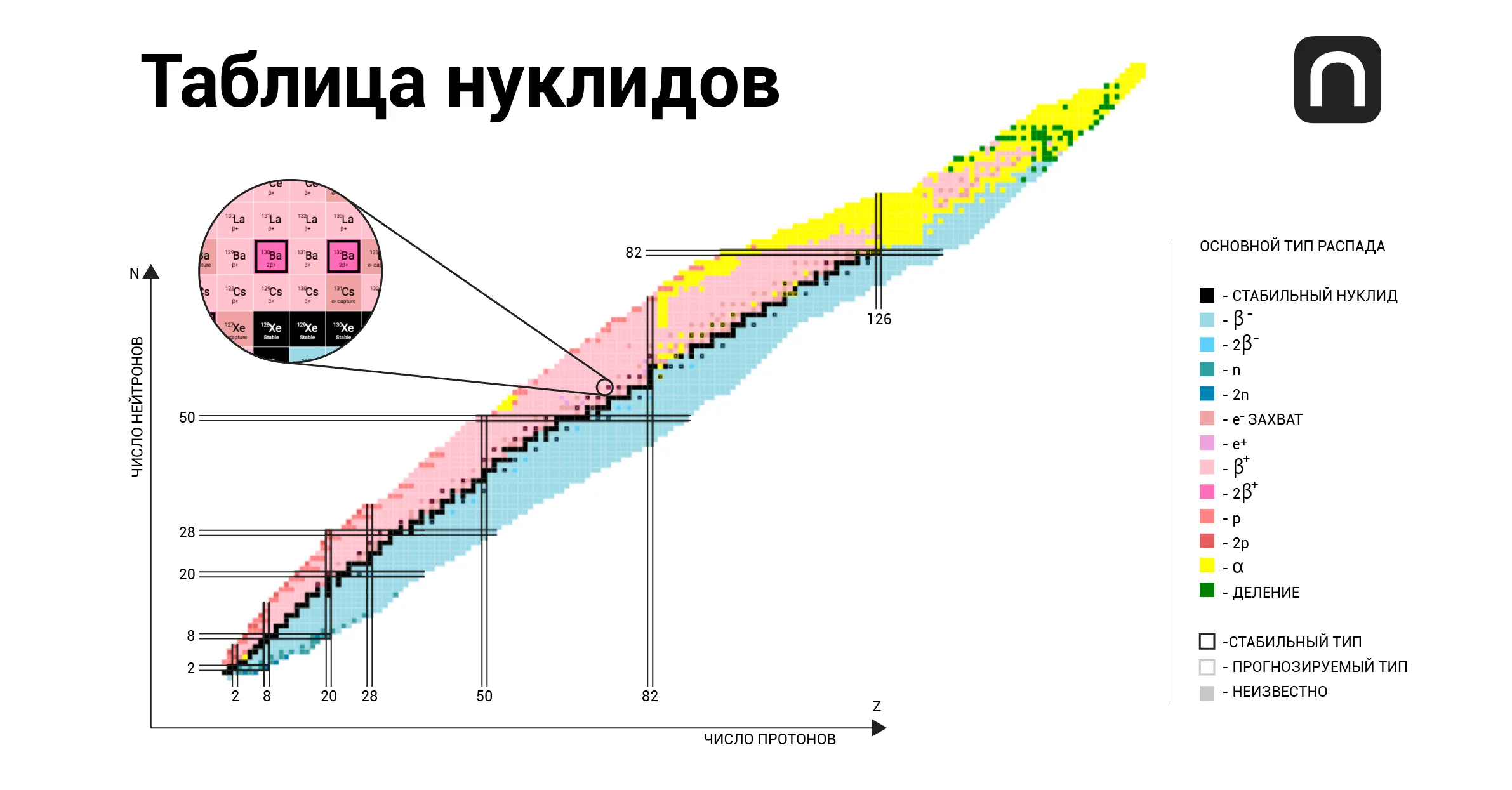
Таблица химических элементов Менделеева постоянно пополняется. Сегодня в ней уже 118 элементов. Впрочем, говоря об изотопах, нужно сверяться уже не с таблицей Менделеева, а с картой нуклидов.
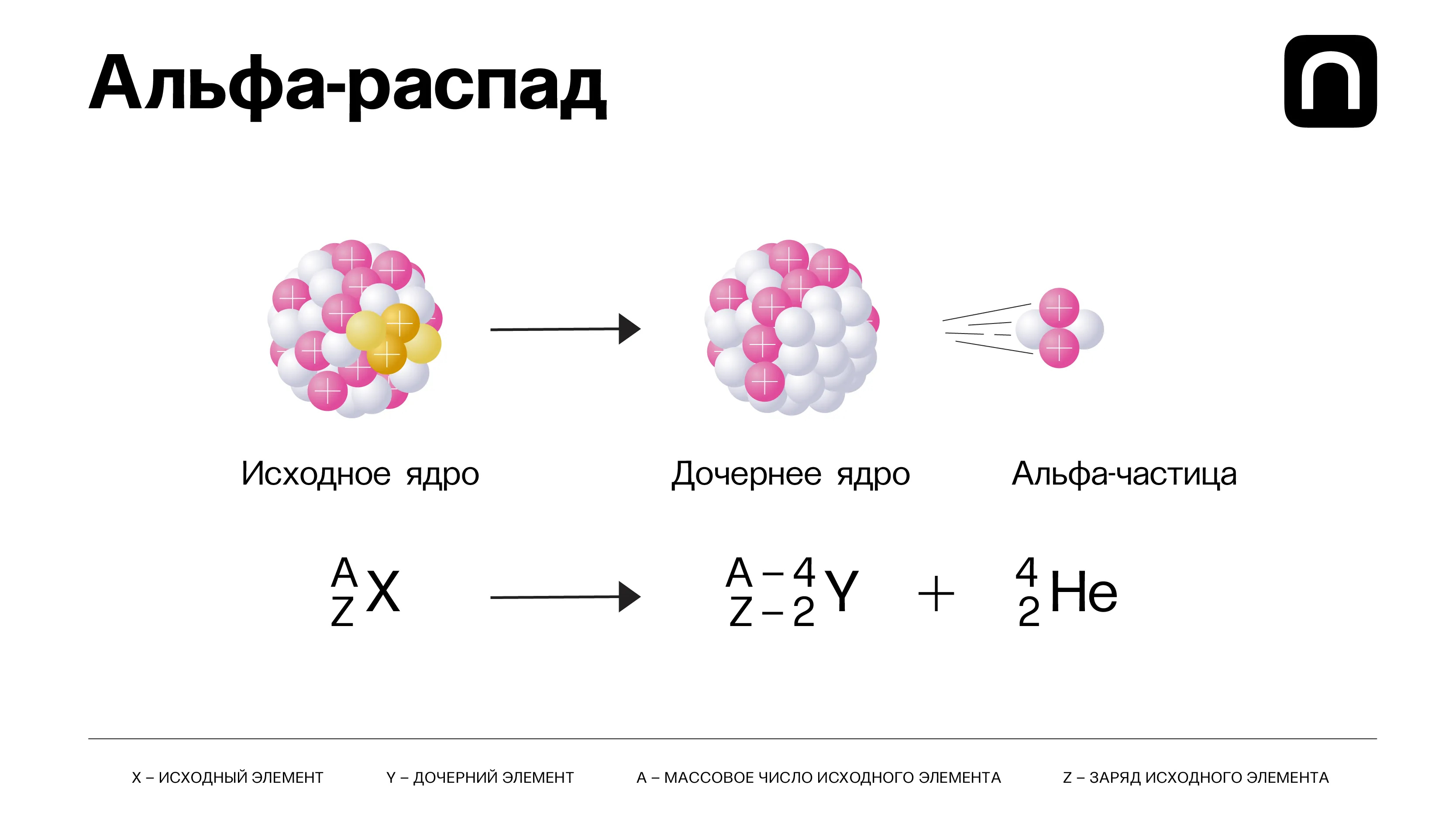
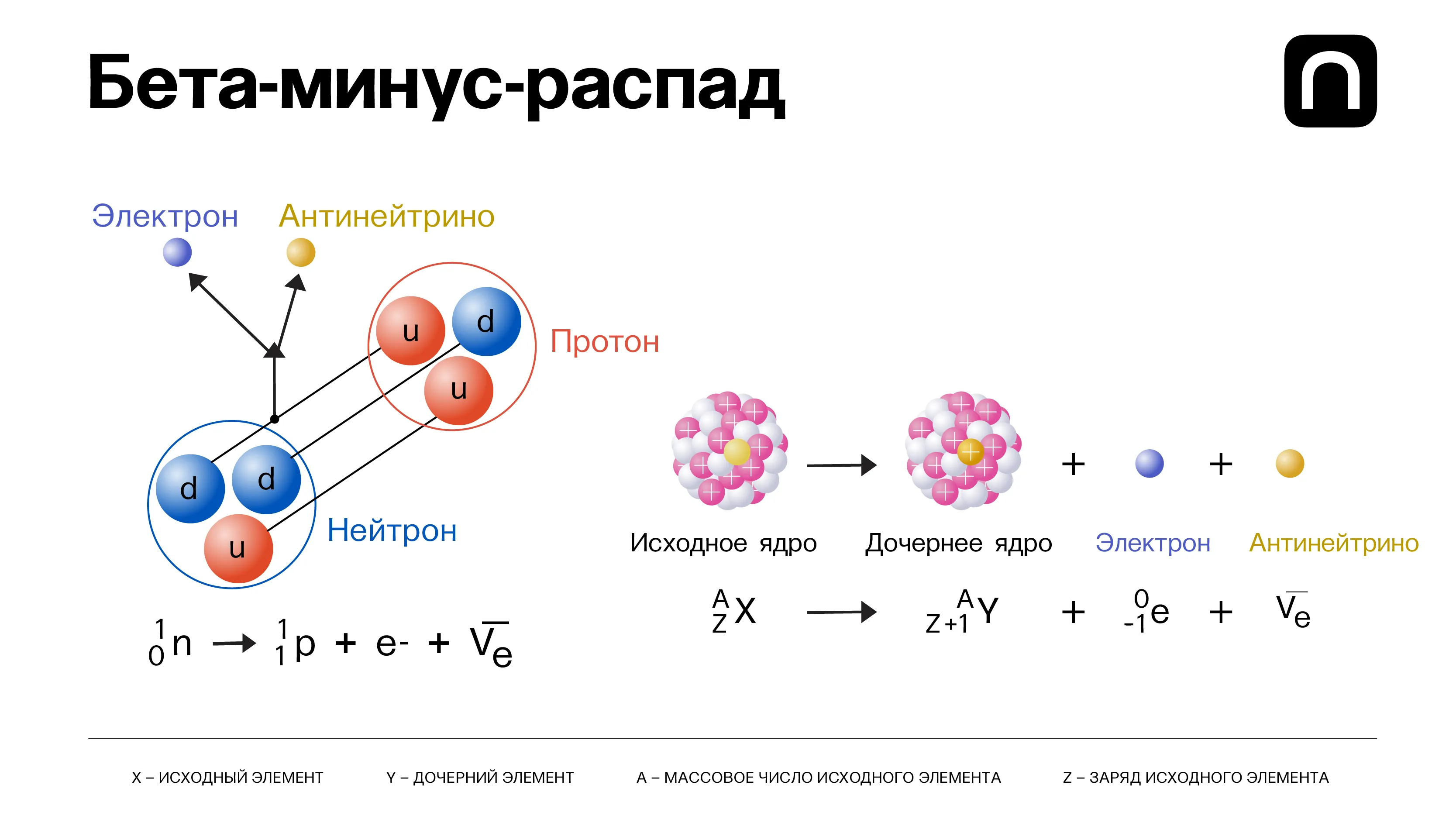
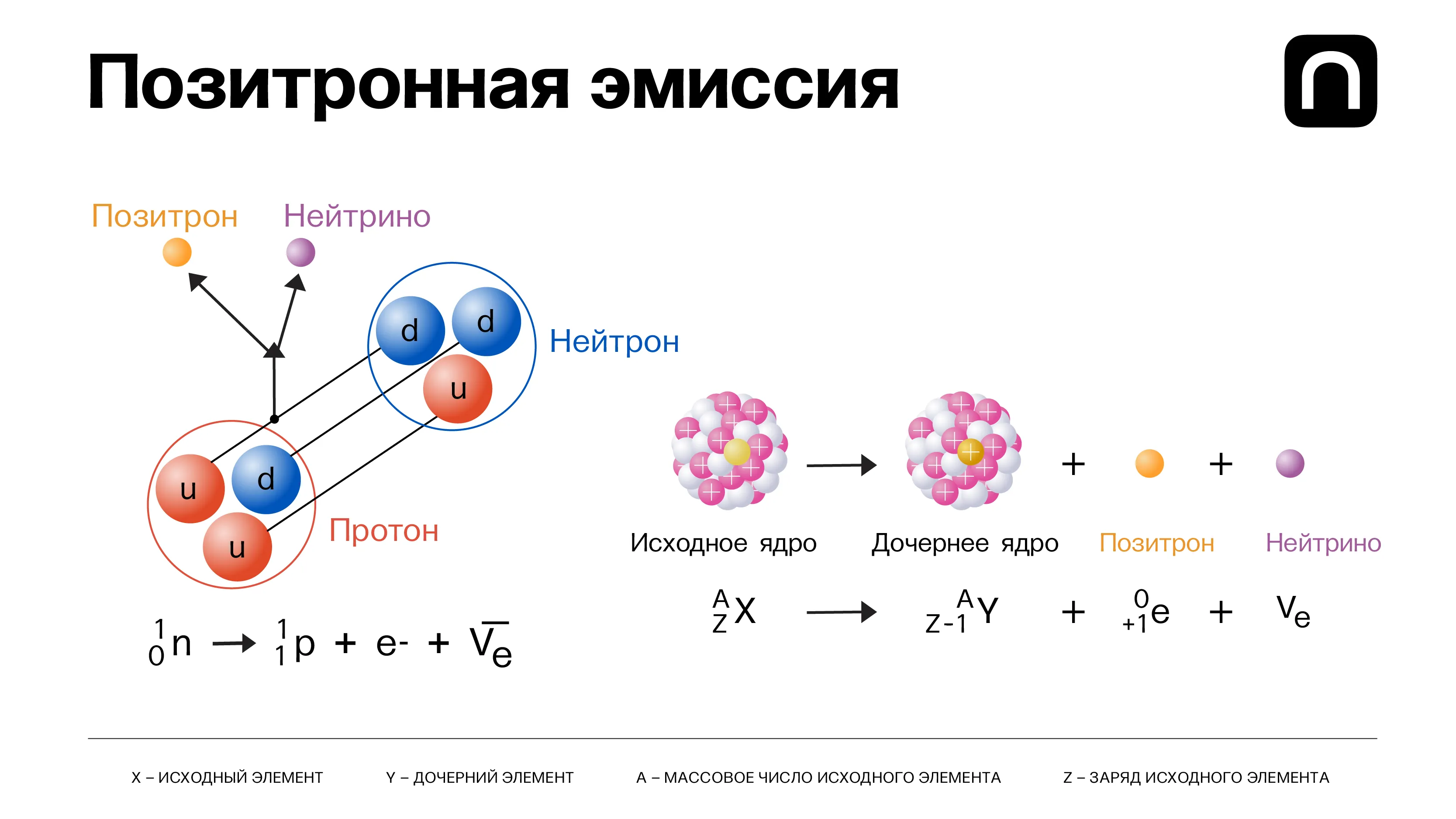
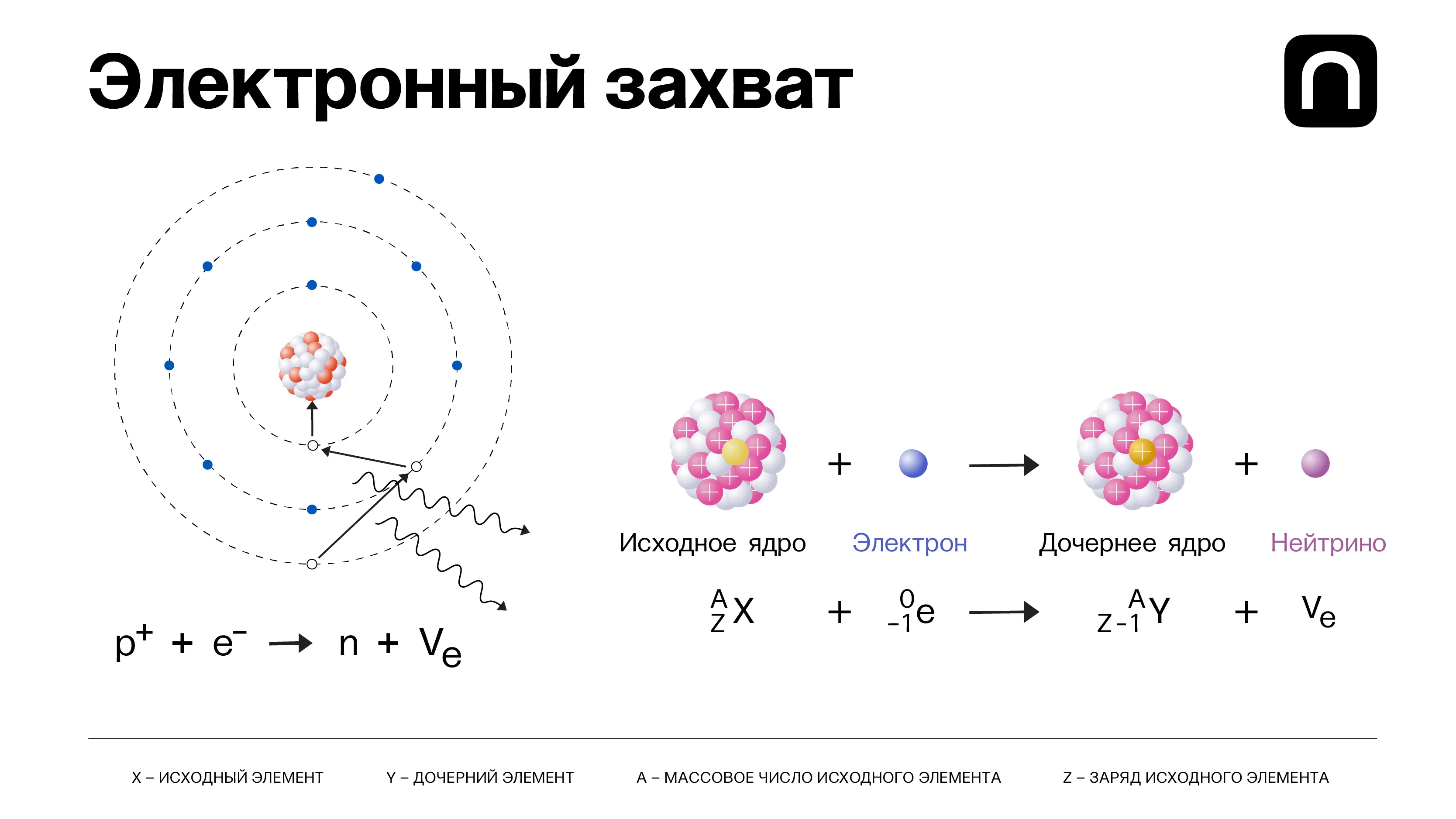
В этой таблице все известные науке нуклиды расположены по осям Z и N, где Z — число протонов, а N — число нейтронов в ядре. Каждая строка — один химический элемент. Черные квадраты — стабильные изотопы, голубая область — бета-минус-распад, рыжая — в основном бета-плюс-распад и электронный захват, К-захват (разновидность бета-распада). Желтая область — альфа-распад, зеленая — спонтанное деление. Об этом будет рассказано далее.
Таким образом, радиоактивных элементов, на текущий момент изученных людьми, гораздо больше, чем имеющих стабильные изотопы (118 против 82): стабильных изотопов около 270, а радиоактивных — уже более двух тысяч.